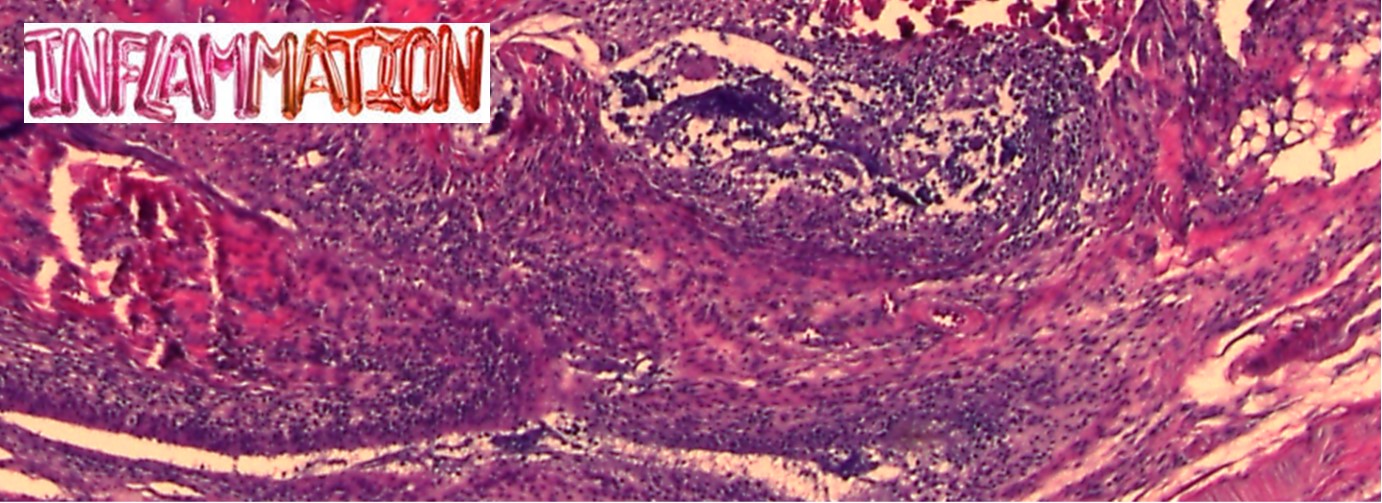
Ερευνητικά πεδία:
Ανοσολογία / Προτυποποίηση φλεγμονωδών και νευροεκφυλιστικών ασθενειών/ Ρευματοειδής Αρθρίτιδα (RA) / Σκλήρυνση κατά Πλάκας (MS) / Alzheimer / προκλινική έρευνα
Συνδυάζουμε την γνώση μας σε τρεις διαφορετικούς κλάδους της Βιοϊατρικής Έρευνας, στην:
– Ανοσολογία: εστιαζόμαστε στη μελέτη των κυτταροκινών IFN τύπου Ι και TNF που αποτελούν βασικούς θεραπευτικούς στόχους φλεγμονωδών νόσων, κυρίως αυτοάνοσων, όπως σκλήρυνσης κατά πλάκας (MS) και ρευματοειδούς αρθρίτιδας (RA) αντίστοιχα.
– Διαγονιδιακή τεχνολογία για την προτυποποίηση ανθρώπινων ασθενειών και
– Επιστήμη των Ζώων (LAS).
Οι γνώσεις μας στη βασική έρευνα μεταφέρονται σε μεταφραστικό επίπεδο, μέσω επιχορηγούμενων εμπιστευτικών ερευνητικών προγραμμάτων με διεθνείς και εθνικές ιδιωτικές φαρμακευτικές εταιρείες.
- Προκλινικές ερευνητικές μελέτες
 διαφόρων αντι-ΤΝF παραγόντων
διαφόρων αντι-ΤΝF παραγόντων
και φυσικών προϊόντων
χρησιμοποιώντας ζωικά πρότυπα πολυαρθρίτιδας
-
- Μελέτη των κυτταρικών και μοριακών μηχανισμών
 των σηματοδοτικών μονοπατιών της IFN-β στην Πειραματική Αυτοάνοση Εγκεφαλομυελίτιδα,
των σηματοδοτικών μονοπατιών της IFN-β στην Πειραματική Αυτοάνοση Εγκεφαλομυελίτιδα,
ΠΑΕ, το ζωικό πρότυπο της σκλήρυνσης
κατά πλάκας, ΣΚΠ.
- Μελέτη των κυτταρικών και μοριακών μηχανισμών
Ερευνητικές Συνεργασίες
– Νόσος Alzheimer
– Γήρανση
– Νευρομυϊκές Ασθένειες
- 53 εμπιστευτικές ερευνητικές μελέτες με διεθνείς και εθνικές ιδιωτικές φαρμακευτικές εταιρείες από το 1996
- Εθνικά Έργα Έρευνας και συνεργατικά ερευνητικά προγράμματα, κυρίως με την ακαδημαϊκή κοινότητα
2018-2020: Πράξη «ELI – LASERLAB Europe Synergy, HiPER & IPERION-CH.gr» HELLAS CH (MIS 5002735)
Δείτε το κείμενο της πράξης εδώ
ΤΡΕΧΟΥΣΕΣ ΔΙΠΛΩΜΑΤΙΚΕΣ ΕΡΓΑΣΙΕΣ
Παπαδημητρίου Α., Μεταπτυχιακή Διπλωματική Εργασία (2018-2019), Τμήμα Βιολογίας, Πανεπιστήμιο Αθηνών
Ρήγκου Α., Μεταπτυχιακή Διπλωματική Εργασία (2017-2018), Τμήμα Βιολογίας, Πανεπιστήμιο Αθηνών
ΕΚΠΑΙΔΕΥΘΕΝΤΕΣ ΣΕ ΠΡΟΠΤΥΧΙΑΚΟ ΚΑΙ ΜΕΤΑΠΤΥΧΙΑΚΟ ΕΠΙΠΕΔΟ
Ηλιοπούλου E., Προπτυχιακή Διπλωματική Εργασία (2017-2018)
Αποκότου O., Προπτυχιακή Διπλωματική Εργασία (2016-2017)
Τσάκα Γ., Προπτυχιακή Διπλωματική Εργασία (2016-2017)
Ιωακειμίδης Φ. -Μεταδιδάκτορας (2016-2017)
Σμπώκου E., Προπτυχιακή Διπλωματική Εργασία (2015-2016)Μαντά A., Πρακτική Άσκηση (2005)
Πουλόπουλος Γ., Μεταπτυχιακή Διπλωματική Εργασία (2013-2014)
Μαρκογιαννάκη M., Προπτυχιακή Διπλωματική Εργασία / Επιστημονικός Συνεργάτης (2012-2013)
Μαλακτάρη Ε., Προπτυχιακή Διπλωματική Εργασία / (2010-11/2013-2016)
Γρίβας Ι., Μεταπτυχιακή Διπλωματική Εργασία / Διδακτορική Διατριβή/ (2010-2015)
Καβροχωριανού Ν., Προπτυχιακή Διπλωματική Εργασία / Διδακτορική Διατριβή/ (2006-2015)
Μωραΐτη Λ., Προπτυχιακή Διπλωματική Εργασία (2008-2009))
Μαντά Α., Πρακτική Άσκηση (2005)
2017
Mavroeidi P., Mavrofrydi O., Pappa E., Panopoulou M., Papazafiri P., Haralambous S., and Efthimiopoulos S. Oxygen and Glucose Deprivation Alter Synaptic Distribution of Tau Protein: The Role of Phosphorylation. Journal of Alzheimer’s Disease, 60 (2017) 593–604.
2016
Alé A., Bruna J., Calls A., Karamita M., Haralambous S., Probert L., Navarro X., Udina E. Inhibitionofthe neuronal NFκB pathway attenuates bortezomib-induced neuropathy in a mouse model. Neurotoxicology, Jul; 55:58-64.
Kavrochorianou N., Markogiannaki M., and Haralambous S. IFN-β differentially regulates the function of T cell subsets in MS and EAE. Cytokine and Growth Factor Reviews 30:47-54, (invited)
Kavrochorianou N., Evangelidou M., Markogiannaki M., Tovey M., Thyphronitis G. and Haralambous S. IFNAR signaling directly modulates T lymphocytes activity resulting in milder Experimental Autoimmune Encephalomyelitis development. Journal of Leukocyte Biology 99(1): 175-88.
2015
Kavrochorianou N., Markogiannaki M., Malaktari E., Tovey M., Thyphronitis G., Haralambous S. An Unknown T cell-associated protective role of IFN-I in the development of Experimental Autoimmune Encephalomyelitis (EAE). Cytokine 76(1): 95.
2013
Kavrochorianou N., Markogiannaki M., Thyphronitis G., Haralambous S. A beneficial effect of type I interferon signaling in T cells in the early phase of experimental autoimmune encephalomyelitis (EAE). Cytokine 63(3): 276.
2012
Kavrochorianou N., Evangelidou M., Tovey M., Thyphronitis G., Haralambous S. The immunomodulatory effect of type I interferon signaling in T cells during EAE. Cytokine 59(3): 574.
2011
Tseveleki V., Badounas F., Kavrochorianou N., Haralambous S. Testing the effect of grey mullet bottarga as a dietary supplement in the development and progression of hypercholesterolemia in genetically modified mice that model atherosclerosis in humans. 15th International Symposium on Atherosclerosis and Related Risk Factors " organized by the Greek Cardiology and held at the National Research Institute on November 25, 2011.
2010
Kavrochorianou N., Evangelidou M., Tovey M., Thyphronitis G., and Haralambous S. Lymphoid tissue- specific overexpression of IFNAR1 in mice for the evaluation of the role of IFNα/β. Transgenic Research 19 (2): 335
Ioannou K., Samara P., Kavrochorianou N., Bega C., Thyphronitis G., Haralambous S., Tsitsilonis O. The C-Terminal decapeptide of prothymosinα induces a TH1-Type immune response in vitro and retards tumor growth in vivo. Proceedings of the 8th Joint Conference of the International Cytokine Society and the international Society for Interferon and cytokine research. Cytokine 52 (1-2): 47-50
2009
Kavrochorianou N., Evangelidou M., Tovey M., Thyphronitis G. and Haralambous S. A transgenic animal model for the investigation of the role of type I interferons in T lymphocyte biology. Cytokine 48(1-2): 47-48.
2008
Mattheolabakis G., Taoufik E., Haralambous S, Roberts ML, Avgoustakis K. In vivo investigation of tolerance and antitumor activity of cisplatin-loaded PLGA-mPEG nanoparticles. Eur J Pharm 71(2): 190-195.
Quinones P., Kalkonde Y., Estrada CA., Jimenez F., Ramirez R., H. Martinez, Mack M., Reddick L., Maffi S., Haralambous S., Probert L., Ahuja K., Ahuja S. Role of Astrocytes and Chemokine Systems in Acute TNF induced Demyelinating Syndrome: CCR2-dependent Signals promote Astrocyte Activation and Survival via NF-B and Akt. Mol. Cell Neurosc. 37(1): 96-109.
Taoufik E., Tseveleki V., Euagelidou M., Emmanouil M., Voulgari-Kokota A., Haralambous S., and Probert L. Positive and negative implications of TNF neutralization for the pathogenesis of multiple sclerosis. Neurogenerative diseases 5(1): 32-7
2005
Hayer S., Toshidast-Akrad M., Haralambous S. Jahn-Schmid B., Skriner K., Trembleau S., Dumortier H., Pinol-Roma S., Redlich K., Schett G., Muller S., Kollias G., Smolen J. and Steiner G. Aberrant Expression of the Autoantigen Heterogeneous Nuclear Ribonucleoprotein-A2 (RA33) and Spontaneous Formation of Rheumatoid Arthritis-Associated Anti-RA33 Autoantibodies in TNF-α Transgenic Mice. J. Immunology, 175: 8327-8336.
2004
Douni E., Sfikakis P., Haralambous S., Fernandes P., Kollias G. Attenuation of inflammatory polyarthritis in TNF transgenic mice by diacerein: comparative analysis with dexamethasone, methotrexate and anti-TNF protocols. Arthritis Res Ther.;6(1):R65-R72.
2003
Aidinis V., Plows D., Haralambous S., Armaka M., Papadopoulos P., Kanaki Z., Koczan D., Thiesen J., Kollias G. Functional analysis of an arthritogenic synovial fibroblast. Arthritis Res Ther. 5(3):R140-157.
Hukkanen M., Platts A., Haralambous S., Ainola M., Konttinen T., Kollias G., Polak M. Induction of inducible nitric oxide synthase, argininosuccinate synthase, and GTP cyclohydrolase I in arthritic joints of human tumor necrosis factor-alpha transgenic mice. J Rheumatol. Apr;30(4):652-659.
2002
Redlich K., Hayer S, Maier A., Dunstan R., Tohidast-Akrad M., Lang S., Turk B., Pietschmann P., Woloszczuk W., Haralambous S., Kollias G., Steiner G., Smolen S., Schett G. Tumor necrosis factor alpha-mediated joint destruction is inhibited by targeting osteoclasts with osteoprotegerin. Arthritis Rheum. Mar;46(3):785-792.
2001
Schett G., Hayer S., Tohidast-Akrad M., Schmid J., Lang S., Turk B., Kainberger F., Haralambous S., Kollias G., Newby C., Xu Q., Steiner G., Smolen J. Adenovirus-based overexpression of tissue inhibitor of metalloproteinases 1 reduces tissue damage in the joints of tumor necrosis factor alpha transgenic mice. Arthritis Rheum. Dec; 44 (12):2888-2898.
1999
Neurath F., Hildner K., Becker C., Schlaak F., Barbuleskcu K., Germann T., Schmitt E., Schirmacher P., Haralambous S., Pasparakis M., ZumBuschenfelde M., Kollias G. and. Marker-Hermann E. Methotrexate specifically modulates cytokine production by T cells and macrophages in murine collagen-induced arthritis (CIA): a mechanism for methotrexate-mediated immunosuppression. Clin. Exp. Immunol. 115 (1): 42-55.
1998
Haralambous S., Plows D. and G. Kollias. Attenuation of transgenic TNF-triggered arthritis in t ype I IL-1 receptor knockout mice. Eur. Cyt.Network 9 (3): 421-
Kaymakcalan Z., Haralambous S., Tracey D., Kamen R., Salfed J. and Kollias G. Prevention of Polyarthritis in human TNF transgenic mice by D2E7: A fully human anti-humanTNF monoclonal antibody. Arthritis and Rheum.41(9):390-392 (D2E7 is now in the market known as Humira)
Douni E., Sfikakis P., Haralambous S., Kollias G. Effects of Glucocorticoid and Methotrexate administration on the Tg197 TNF-transgenic mouse model of chronic inflammatory polyarthritis. Arthritis and Rheumatism 41(9):100
1997
Neurath M., Fuss I., Pasparakis M., Alexopoulou L., Haralambous S. , Meyerzum H. Buschenfelde, Strober W. and Kollias G.. Predominant pathogenic role of tumor necrosis factor α in experimental colitis in mice. Eur. J. Immunol. 27:1743-1750.
Platts M., Haralambous S., Hukkanen J., Gross S., Kollias G., Polak M. Inducible nitric oxide synthase and cyclooxygenase are expressed in human-TNFα transgenic mice which develop arthritis spontaneously. J. Pathology 181: A42
Kollias G., Akassoglou K., Alexopoulou L., Douni E., Haralambous S., Hill S., Kassiotis G., Kontoyiannis D., Pasparakis M., Plows D., Probert L. Animal models of TNF-mediated inflammation. J. of Leukocyte Biology p: 9
1996
Probert L., Akassoglou K., Alexopoulou L., Douni E., Haralambous S., Hill S., Kassiotis G., Kontogiannis D., Pasparakis M., Plows D., and Kollias G. Dissection of the pathologies induced by transmembrane and wild type tumour necrosis factor in transgenic mice. Journal of Leucocyte Biology, 59: 518-525.
Haralambous S., Probert L., Mastrangelo M., Kollias G. and Molony L. Adhesion molecule blockade modulates the development of TNF-triggered arthritis in transgenic mice. Eur. Cytokine Netw., 7: 293

